2021年11月,华中科技大学同济医学院附属协和医院刘国辉教授团队的多项研究成果分别于国际一流期刊《Small》(IF:13.281)、《Bioactive Materials》(IF:14.593)、《ACS Applied Materials & Interfaces》(IF:9.229)在线发表。
糖尿病创面的治疗仍然是临床实践中的一大挑战,慢性创面的特征是多重耐药细菌感染、血管病变和微环境氧化损伤。因此,刘国辉教授团队与重庆大学冯茜教授团队合作设计了一种新型的可原位注射HA@MnO2/FGF-2/Exos水凝胶,用于促进糖尿病创面的愈合。通过简单的局部注射,这种水凝胶能够形成覆盖伤口的保护性屏障,提供快速止血和长期抗菌保护。MnO2/ε-P纳米水凝胶能够催化伤口中产生的过量H2O2转化为O2,不仅消除了H2O2的有害影响,而且还为伤口愈合提供了O2。此外,M2型巨噬细胞来源的外泌体(M2 Exosome,M2Exos)和FGF-2生长因子的释放分别刺激血管生成和上皮化。这些体内和体外结果表明,使用HA@MnO2/FGF-2/Exos水凝胶可以加速糖尿病伤口的愈合,为慢性糖尿病伤口修复提供了一种可行的策略。
相关研究成果“ All-in-One: Multifunctional Hydrogel Accelerates Oxidative Diabetic Wound Healing through Timed-Release of Exosome and Fibroblast Growth Factor”11月17日于《Small》在线发表。刘国辉教授和米博斌博士为本文的共同通讯作者,课题组成员熊元博士后、陈朗博士为本文的共同第一作者。

骨折愈合早期,免疫细胞将会被招募至骨折部位,其产生的补体和细胞因子有利于凝血、清除细菌等异物,对于后续的愈合过程必不可少。但是,过度持续的炎症则会对组织形成一定的损伤,从而影响骨折的愈合。因此,抑制骨折部位过度活跃的免疫细胞是一种具有前景的治疗方式。PD-L1 (Programmed cell death 1 ligand 1, 细胞程序性死亡-配体1) 在肿瘤细胞表面高度表达,并与免疫细胞T细胞表面的受体蛋白PD-1结合,从而实现免疫逃逸。由于PD-L1直接作用于免疫细胞,起到抑制免疫反应的作用,因此在除肿瘤以外的炎性疾病中也有很大的研究价值。研究报道,PD-L1在创面修复中起到一定的积极作用。然而,目前对于PD-L1影响骨折修复作用的研究仍处于空白阶段。刘国辉教授团队经前期研究发现了PD-L1在骨折修复过程中发挥了积极的作用。因此,本研究提取了富含PD-L1的外泌体用于促进骨折愈合。同时,刘国辉教授团队同重庆大学冯茜教授团队合作设计合成了可注射HA/Gel水凝胶,用于负载递送并缓释富含PD-L1外泌体。水凝胶对MMP9的敏感特性,也使其可响应炎症反应加速缓释,以更好的抑制免疫反应对骨折断端组织的损伤。本研究发现,外泌体通过PD-L1向骨折部位T细胞发送“Don’t eat me”信号,从而减轻局部的炎症反应,以促进骨折的愈合。本研究对后续进一步研究PD-L1在骨折修复中起到的作用具有一定的探索与指导的意义。
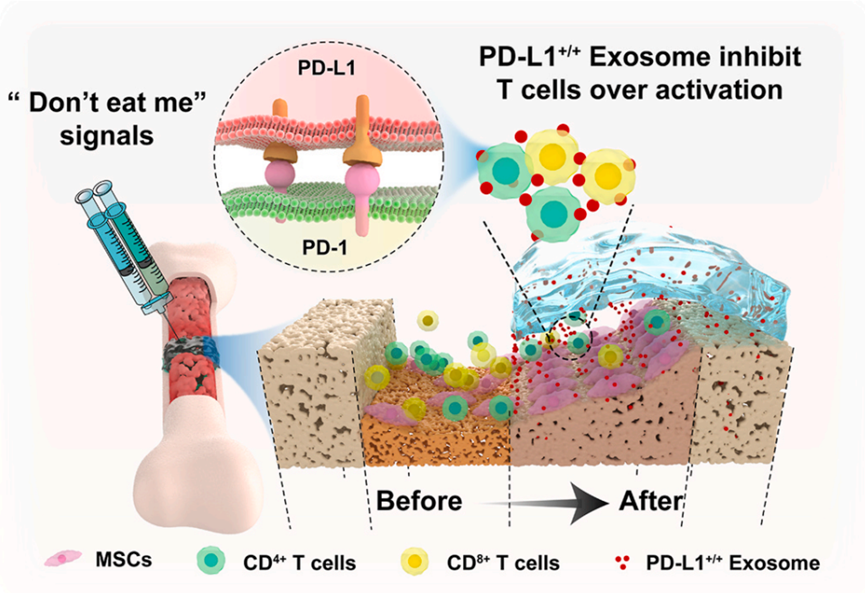
相关研究成果“Exosomal PD-L1 Induces Osteogenic Differentiation and Promotes Fracture Healing by Acting as an Immunosuppressant” 11月3日于《Bioactive Materials》正式线上发表。刘国辉教授和米博斌博士为本文的共同通讯作者,课题组成员林泽硕士、熊元博士后、胡益强博士为本文的共同第一作者。

巨噬细胞作为影响骨重建最重要的免疫细胞之一,主要通过M2型极化发挥促进骨折愈合作用。研究发现,黄芩素(BCL)作为一种中药提取物,具有抗炎、抗氧化、抗癌、抗糖尿病等多种功能,同时对M2型巨噬细胞的极化具有明显的促进作用。然而,由于其存在靶向巨噬细胞的局限性以及全身毒性,很少被应用于骨折的治疗。因此,刘国辉教授团队同武汉科技大学邱文秀教授团队合作制备了一种磁性介孔二氧化硅纳米颗粒(MMSNPs)用于靶向递送黄芩素至骨折部位。环糊精(CD)作为调控黄芩素释放的“看守者”被负载到微粒上。同时,靶向巨噬细胞的NW多肽也被负载于微粒中,与微粒具备的磁靶向形成双重靶向作用。在骨折部位外部磁场的作用下,微粒可以精准地将黄芩素递送至骨折部位的巨噬细胞。在细胞内谷胱甘肽(GSH)的作用下,二硫键被裂解从而CD被去除,黄芩素也得以被释放。本研究表明,黄芩素通过抑制细胞内的ROS/NFκB信号通路,抑制炎症反应,促进骨髓来源的巨噬细胞(BMDM)的M2型极化。从而促进骨髓间充质干细胞(BMSC)的成骨分化,对骨折的愈合起到积极作用。该靶向纳米微粒解决了黄芩素对于骨折部位巨噬细胞靶向性的局限性,同时大大地降低了其对于全身的毒性。
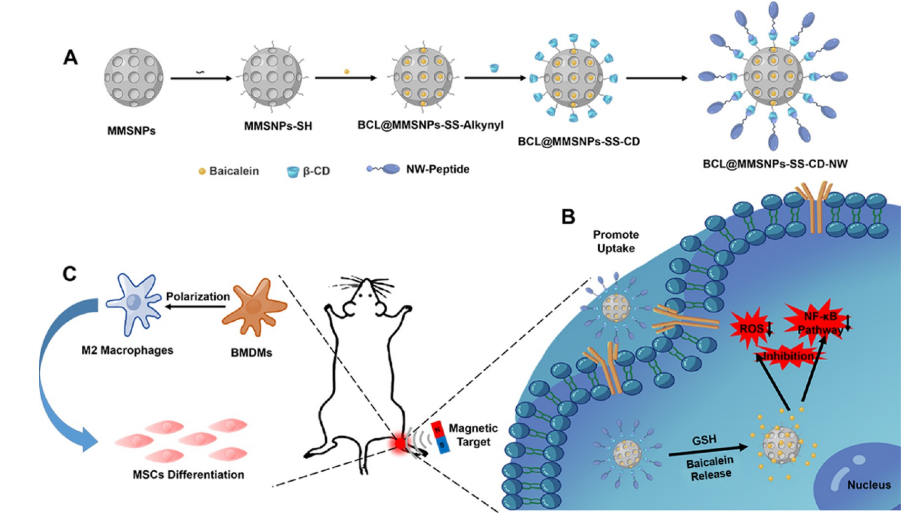
相关研究成果“Dual-Targeted Nanoplatform Regulating the Bone Immune Microenvironment Enhances Fracture Healing”11月19日发表于《ACS Applied Materials & Interfaces》。刘国辉教授和米博斌博士为本文的共同通讯作者,课题组成员周武博士、林泽硕士、熊元博士后为本文的共同第一作者。

刘国辉教授以课题负责人主持国家自然科学基金5项,以课题负责人、项目骨干主持国家重点研发计划项目2项,以第一负责人主持国家卫计委重点研发计划2项、省部级科技基金项目12项,以课题负责人主持湖北省重点研发计划1项,以通讯作者(含第一作者)在国内外权威期刊发表专业论文320余篇,其中SCI论文70余篇。刘国辉教授团队将继续在创面愈合、骨折修复及生物材料的应用方面的研究继续深耕,以为临床带来更好的应用治疗做出努力。(骨科)
论文信息
1、Xiong, Y.; Chen, L.; Liu, P.; Yu, T.; Lin, C.; Yan, C.; Hu, Y.; Zhou, W.; Sun, Y.; Panayi, A. C.; Cao, F.; Xue, H.; Hu, L.; Lin, Z.; Xie, X.; Xiao, X.; Feng, Q.; Mi, B.; Liu, G., All-in-One: Multifunctional Hydrogel Accelerates Oxidative Diabetic Wound Healing through Timed-Release of Exosome and Fibroblast Growth Factor. Small.
2、Lin, Z.; Xiong, Y.; Meng, W.; Hu, Y.; Chen, L.; Chen, L.; Xue, H.; Panayi, A. C.; Zhou, W.; Sun, Y.; Cao, F.; Liu, G.; Hu, L.; Yan, C.; Xie, X.; Lin, C.; Cai, K.; Feng, Q.; Mi, B.; Liu, G., Exosomal PD-L1 induces osteogenic differentiation and promotes fracture healing by acting as an immunosuppressant. Bioact Mater.
3、Zhou, W.; Lin, Z.; Xiong, Y.; Xue, H.; Song, W.; Yu, T.; Chen, L.; Hu, Y.; Panayi, A. C.; Sun, Y.; Cao, F.; Liu, G.; Hu, L.; Yan, C.; Xie, X.; Qiu, W.; Mi, B.; Liu, G., Dual-Targeted Nanoplatform Regulating the Bone Immune Microenvironment Enhances Fracture Healing. ACS Appl Mater Interfaces.