2023年8月25日,协和医院急诊医学科/急诊创伤外科赵刚教授团队在高水平期刊Gastroenterology(IF=29.4)在线发表研究成果,阐明慢性胰腺炎纤维化的调控新机制。华中科技大学同济医学院附属协和医院急诊创伤外科为唯一作者单位,赵刚教授为通讯作者,王德才博士、韩胜博博士、吕国政硕士和胡宇航博士为第一作者。

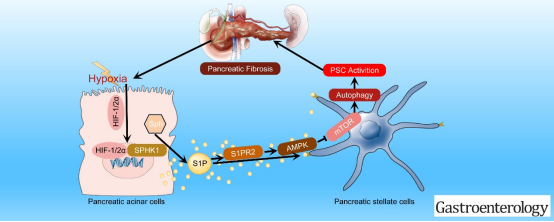
慢性胰腺炎(CP)是一种以胰腺腺泡细胞破坏、进行性纤维化、外分泌和内分泌功能进行性丧失为特征的疾病。活化的胰腺星状细胞(PSCs)被认为是胰腺纤维化恶化的关键调节因子。PSCs的自噬是CP纤维形成的调节枢纽。然而,在CP过程中PSCs自噬活性增加的机制仍不确定。研究分析了受损胰腺腺泡细胞(iPACs)在CP的PSCs活化中的作用。结果表明,CP小鼠胰腺组织损伤胰腺腺泡细胞(iPACs)和腺泡细胞中SPHK1/S1P显著升高。同时,在SPHK1-/-小鼠和rAAV-SPHK1-KD小鼠中,CP的发病、纤维化和PSCs活化均被明显抑制。同时,iPACs明显激活PSCs,而SPHK1敲低后则可逆转。iPACs衍生的S1P特异性结合PSCs的S1PR2,从而调节AMPK/mTOR通路,诱导PSCs自噬和活化。HIF-1α和HIF-2α在缺氧条件下促进PACs的SPHK1转录,这是CP微环境的显著特征。同样,抑制剂PF-543和JTE-013抑制SPHK1和S1PR2活性明显阻碍了CP小鼠胰腺纤维的形成。综上,iPACs中活化的SPHK1/S1P通路通过调控S1PR2/AMPK/mTOR通路诱导自噬和PSCs活化,促进CP的纤维化发生,缺氧微环境可能参与了PACs与PSCs在CP发病中的相互作用。该研究强调了缺氧/SPHK1/S1P/S1PR2信号介导的CP损伤PACs和活化PSCs之间串扰的重要性,为CP的治疗提供了新的治疗靶点和新的治疗思路,也将推动下一步CP的临床转化研究。
原文链接:https://www.gastrojournal.org/article/S0016-5085(23)04912-0/fulltext
Gastroenterology是消化系统疾病领域著名的Top期刊,由美国胃肠病学会(AGA)主办,涵盖了消化系统疾病的各个方面,包括胃肠道疾病的发病机制、诊断、治疗和预防等。该期刊的影响因子在消化病学领域内排名第一,非常注重原创文章的创新性。
赵教授团队一直致力于胰腺肿瘤与急慢性胰腺炎等疾病的分子机制与治疗研究,从分子层面出发,探索疾病发生机制与治疗新策略,旨在造福广大患者。团队已累计发表SCI论文30余篇,其中影响因子IF>10 的 8 篇,IF>7 的8篇,IF>5 的 11 篇(包括 Cancer Research等肿瘤领域权威期刊)。本次发表胃肠病领域TOP期刊论文,也是团队新的突破。
通讯作者:赵刚教授目前担任协和医院急诊医学科主任、急诊创伤外科主任。三级教授,主任医师,博士后导师。武汉市中青年骨干医学专家,华中卓越学者特聘专家,留德博士后。获湖北省科技进步一等奖2次,中华医学会二等奖1次,中华医学会三等奖1次,教育部科技进步二等奖1次,武汉市科技进步一等奖1次。主持国家自然科学基金7项,华中科技大学临床研究项目3项,发表SCI论文50余篇。参与编写胰腺癌诊治指南和专家共识 4 部。获中国急诊医师协会突出贡献奖等荣誉。目前兼任湖北省医学会肠外与肠内营养分会副主任委员等职务。担任中华外科杂志、World Journal of Emergency Medicine等多种中外期刊编委。